Какая кислота в аккумуляторе автомобиля и для чего нужен электролит
Содержание:
- Приготовление электролита
- Процессы, происходящие в АКБ с участием электролита
- Как самостоятельно приготовить электролит для аккумулятора
- Как сделать электролит в домашних условиях?
- Серная кислота в аккумуляторе
- Полная замена электролита в аккумуляторе
- Процесс приготовления электролита
- Нейтрализация электролита
- Какая кислота используется в автомобильных аккумуляторах
Приготовление электролита
Для приготовления электролита обязательна подготовка инструмента и средств защиты.
Средства защиты:
- резиновые перчатки;
- фартук и нарукавники устойчивые к агрессивным химическим реактивам;
- защитные очки;
- кальцинированная сода или другая щелочь для нейтрализации.
Инструменты и материалы:
- стеклянная или другая емкость устойчивая к кислоте;
- стеклянный термометр для измерения температуры раствора;
- ареометр или денсиметр для измерения плотности жидкостей;
- палочка для перемешивания жидкости;
- дистиллированная вода;
- серная кислота.
Серная кислота в аккумуляторе выпускается по ГОСТ 2184-77 или ГОСТ 14262-78. Эти стандарты оговаривают концентрацию, количество примесей и другие технические условия. Часто для АКБ продается уже готовый для употребления электролит
Здесь следует обратить внимание на то для каких условий он приготовлен
Для дистиллированной воды используется ГОСТ 6709-72.

Кроме материалов и средств защиты важна последовательность действий при приготовлении:
- определяется плотность серной кислоты;
- в приготовленную емкость заливается нужное количество воды;
- аккуратно, тонкой струйкой, заливаем кислоту в воду;
- аккуратно перемешиваем полученный состав;
- даем ему остынуть и отстояться в течении нескольких часов.
При работе с кислотой следует выполнять все меры безопасности:
- Работы проводим в хорошо проветриваемом помещении.
- В случае пролива обязательно нейтрализуйте ее щелочью.
- Опасайтесь попадания на лицо или одежду.
- Нельзя вдыхать пары – они могут привести к ожогам легких или верхних дыхательных путей.
- Попадание кислоты в глаза может привести к слепоте. В этом случае обязательно промойте глаза большим количеством воды и сразу обратитесь к врачу.
Процессы, происходящие в АКБ с участием электролита
Работа свинцово-кислотного автомобильного аккумулятора основывается на электрохимических процессах, которые протекают с участием электролита. Аккумулятор автомобиля состоит из положительных и отрицательных пластин, погруженных в водный раствор серной кислоты. Положительные и отрицательные пластины имеют токоотводящие решётки из свинца с различными добавками в зависимости от типа аккумулятора. На решётках положительных электродов нанесён красновато-коричневый диоксид свинца (PbO2). На отрицательных электродах — сероватый порошок свинца (Pb). Электрические характеристики аккумулятора напрямую зависят от плотности электролита. Для понимания назначения электролита нужно рассмотреть основные процессы, происходящие в аккумуляторе автомобиля.
При разряде аккумулятор на положительном электроде (аноде) идёт следующая реакция:
PbO2 + SO42− + 4H+ + 2e− -> PbSO4 + 2H2O
На отрицательном электроде (катоде) протекает такой процесс:
Pb + SO42− − 2e− ->PbSO4
При заряде АКБ эти реакции протекают в обратном направлении. Электролит в свинцово-кислотном автомобильном аккумуляторе имеет разную плотность в зависимости от степени заряженности АКБ. Как уже говорилось выше, концентрированная кислота аккумуляторного сорта имеет плотность 1,835 гр/см3. Плотность электролита на заряженном аккумуляторе лежит в диапазоне 1,127─1,300 гр/см3. При разрядке аккумулятора автомобиля в результате электрохимической реакции из электролита расходуется серная кислота и его плотность падает. Пока через батарею проходит ток разряда кислота рядом с электродами расходуется в результате вышеописанной реакции. Идёт диффузия H2SO4 из объёма к электродам. Таким образом, поддерживается напряжение на выводах аккумулятора. В начале разрядки процесс диффузии кислоты в электроды. Это объясняется тем, что в активной массе электродов поры ещё не забиты сульфатом. По мере того, как на них образуется слой сульфата и забивает поры, процесс диффузии притормаживается. В теории процесс разряда может идти до того момента, пока электролит не превратится в воду. Но на практике разряд идёт до тех пор, пока плотность не опуститься до значения 1,15 гр/см3. К моменту падения плотности до 1,15 гр/см3 выделяется столько сульфата свинца, что его хватило для закупоривания активной массы пластин. По плотности электролита можно судить о степени заряженности АКБ. Для этого можно использовать таблицу, представленную ниже.
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
| 1,11 | 11,7 | 8,4 | -7 | |
| 1,12 | 11,76 | 8,54 | 6 | -8 |
| 1,13 | 11,82 | 8,68 | 12,56 | -9 |
| 1,14 | 11,88 | 8,84 | 19 | -11 |
| 1,15 | 11,94 | 9 | 25 | -13 |
| 1,16 | 12 | 9,14 | 31 | -14 |
| 1,17 | 12,06 | 9,3 | 37,5 | -16 |
| 1,18 | 12,12 | 9,46 | 44 | -18 |
| 1,19 | 12,18 | 9,6 | 50 | -24 |
| 1,2 | 12,24 | 9,74 | 56 | -27 |
| 1,21 | 12,3 | 9,9 | 62,5 | -32 |
| 1,22 | 12,36 | 10,06 | 69 | -37 |
| 1,23 | 12,42 | 10,2 | 75 | -42 |
| 1,24 | 12,48 | 10,34 | 81 | -46 |
| 1,25 | 12,54 | 10,5 | 87,5 | -50 |
| 1,26 | 12,6 | 10,66 | 94 | -55 |
| 1,27 | 12,66 | 10,8 | 100 | -60 |
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
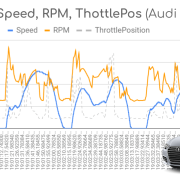
Полностью заряженный элемент АКБ автомобиля выдаёт напряжение 2,5─2,7 вольт без нагрузки на выводах. При подключении нагрузки напряжение проседает до 2,1 вольта за несколько минут. За это время успевает сформироваться слой PbSO4 на поверхности отрицательных электродов. То есть, напряжение одного элемента на подключённой к автомобилю АКБ составляет примерно 2,15 вольта. Если разряжать аккумулятор автомобиля небольшим током (10 процентов от номинальной ёмкости), то через час разрядки напряжение элемента снижается до 2 вольт. Это происходит из-за того, что в этом момент быстро формируется большое количество PbSO4, который забивает поры активной массы. В результате растёт внутреннее сопротивление элементов АКБ и падает концентрация электролита. Через некоторое время процесс разрядки выходит на прямую (см. график).

График разрядки аккумулятора Эта прямая соответствует балансу плотностью электролита около электродов и в остальном объёме. Постепенно кислота поступает из объёма к электродам и вступает в реакцию с выделением сульфата свинца. Плотность электролита постепенно снижается, а напряжение падает медленнее, чем на начальной стадии. И на конечной стадии, когда активная масса блокируется образовавшимся сульфатом свинца, реакция замедляется и напряжение быстро падает.
Как самостоятельно приготовить электролит для аккумулятора
Если средства индивидуальной безопасности, измерительные приборы и материалы приготовлены, можно приступать к смешиванию компонентов. Готовую жидкость рекомендуется сразу залить в АКБ, в крайнем случае – отнести в гараж. Разумеется, первый вариант предпочтительнее, поскольку хранение батареи без электролита приводит к деградации и разрушению активной массы электродов.
Рассмотрим, как приготовить электролит для кислотно-свинцовых аккумуляторов
Помещение, в котором вы будете работать, должно быть вентилируемым, температура не должна превышать 25° С. Аккумуляторы, используемые в легковом транспорте – это 55–60-амперные батареи, в которые помещается до 3.7 литра электролита (при желании эту цифру можно уточнить на сайте производителя). Чтобы перестраховаться, изготавливаем жидкости на 300–400 мл больше требуемого. До начала приготовления раствора необходимо определиться с его плотностью. Выше мы указали допустимый диапазон, а конкретное значение зависит от климата региона, в котором вы проживаете. Если это юг, то значение должно быть близким к минимальному порогу, с продвижением на север начальная плотность должна расти.

Так, для Крайнего Севера, где зимой возможны 50-градусные морозы, плотность должна соответствовать значению 1.27 г/см3, причём после заливки и зарядки батареи она поднимется до 1.29 г/см3. В средних широтах делаем электролит плотностью 1.28 г/см3.
Как и плотность, пропорции состава электролита для аккумуляторов будут зависеть от региона. Так, для юга, чтобы получить плотность 1.24 г/см3, нам потребуется на 1 литр дистиллированной воды 330 мл серной кислоты.
Алгоритм приготовления раствора для свинцовых аккумуляторов в домашних условиях:
- наливаем в подготовленную ёмкость необходимое количество дистиллированной воды;
- тонкой струёй начинаем добавлять кислоту, одновременно помешивая жидкость стеклянной палочкой;
- после окончания процесса производим замер плотности и оставляем раствор на 12 часов для окончательного перемешивания компонентов. Измеряем плотность повторно, если имеется расхождение с расчётной величиной, добавляем соответствующий компонент;
- готовый электролит заливаем в банки АКБ, которую предварительно желательно промыть. Снова замеряем плотность и при необходимости производим корректировку, доливая воду или кислоту.
Окончательный замер производится на полностью заряженном аккумуляторе.
Процесс приготовления электролита на щелочной основе
Щелочной электролит может продаваться в виде готового раствора или в гранулах. Последние засыпаются в дистиллированную воду, и жидкость стеклянной палочкой размешивается до полного растворения щёлочи. В какой пропорции брать компоненты, обычно указывается на этикетке аккумулятора, наклеенной на его боковой грани.

Ситуация с плотностью щелочного электролита аналогична кислотному: чем ниже температура эксплуатации автомобиля, тем выше должна быть долевая часть более тяжёлой щёлочи. Так, при температуре до 20 градусов ниже нуля практикуется использование раствора плотностью 1.21 г/см3.. При его приготовлении необходимо добавить 20 г гранул на литр щёлочи.
Если предполагается использование АКБ при температурах до -40 градусов, плотность электролита нужно повысить до 1.28 г/см3.
Приведём распространённые рецепты приготовления щелочного электролита:
- для плотности в пределах 1.17–1.19 г/см3 необходимо взять на одну часть щёлочи четыре части дистиллированной воды;
- плотность 1.19–1.21 г/см3 достигается при пропорциях 1 часть щелочи к двум частям воды;
- плотность 1.27 г/см3, которая позволяет получить жидкость, не застывающую при очень низких температурах, достигается при смешивании воды и щёлочи в одинаковых пропорциях.
Чтобы правильно приготовить щелочной электролит, после смешивания его необходимо выдержать в течение 6–8 часов для полноценного перемешивания в закрытой крышкой ёмкости. Контакт с атмосферным воздухом нежелателен – он оказывает деградирующее воздействие на электролит. Незначительная часть щёлочи обычно не растворяется, выпадая в осадок. В аккумулятор следует заливать только прозрачную жидкость, без примесей, которые становятся причиной замыкания пластин и увеличения тока саморазряда.
Как сделать электролит в домашних условиях?
Рекомендуем купить его в магазине, но его можно сделать и своими руками.
Нам потребуются:
- Дистиллированная вода;
- Серная кислота;
- Емкость из стекла, керамики или свинца, устойчивая к кислотам;
- Эбонитовая палочка.
Чтобы сделать электролит надо залить воду в специальную емкость и добавить туда серную кислоту в пропорции 3:1. Тщательно перемешать смесь эбонитовой палочкой. Вещество плотно накрыть и оставить на 1 день до выпадения осадка.
 Таблица для расчета приготовляемого электролита
Таблица для расчета приготовляемого электролита
Необходимо сказать, что превышения в допустимой концентрации электролита может привести к самым неприятным последствиям. От чрезмерно концентрированного вещества пластины аккумулятора очень быстро «разъест», что в кратчайшие сроки вызовет выход аккумулятора из рабочего состояния.
 В дист вода добавляем кислоту, а не наоборот
В дист вода добавляем кислоту, а не наоборот
А вот слишком низкий уровень плотности вещества может очень быстро вызывать сульфатацию. Наверняка вы знаете, что это такое. Нет? Это процесс оседания кристаллических осадков на пластинах, в результате чего аккумулятор теряет свои свойства и просто оказывается неспособным держать заряд долгое время.
К чему приведёт нарушение рецептуры
Самые большие значения параметров электролита необходимо смешивать, а не добавлять их сразу в аккумулятор. Электролитическая жидкость с большой концентрацией может привести к неприятным последствиям.
Из-за низкой разбавленности начинают в первую очередь разъедаться металлические пластины. Поэтому после того, как автовладелец добавит сильный концентрат электролита, он не должен удивиться тому, что аккумуляторная батарея испортилась.
Если параметр плотности будет слишком низким, то это вызовет известный процесс, который носит название — сульфатация.
Во время такого процесса происходит накопление сульфитов свинцового металла, что мешает этому свинцу накапливать необходимое количество заряда. Помимо этого, при сильных морозах низкая концентрация электролита может привести к тому, что он замёрзнет. Процесс сульфатации.
Как измерить и откорректировать плотность электролита
Для измерения и корректировки электролитической жидкости потребуется дополнительный прибор, который называется — ареометр. Автовладельцы обычно используют две разновидности прибора: плавкие и с образованием постоянной массы.Ареометр с постоянной массой, имеет специфический шкалистый поплавок с дополнительным грузом. Если плотность будет низкая, поплавок погрузится на малую глубину. При высокой плотности грузик уйдёт глубоко в электролит.
Стоит учесть, что такой вариант ареометра не подходит в аккумуляторные батареи автомобиля, из-за того, что у него нет дополнительного шприца. Он нужен для забора электролита. Многопоплавковая разновидность имеет несколько грузиков, которые плавают на поверхности смеси.
Также как и с предыдущим вариантом, глубина зависит от количества плотности электролитической жидкости.
Огромным и важным минусом данной модели является то, что его измерения бывают достаточно не точными.
Теперь с плотностью всё понятно, можно перейти к приготовлению раствора электролитической жидкости. Чтобы это сделать потребуется, как уже упоминалось, дистиллированный раствор и серная кислота. Найти каждый из этих компонентов не составит труда.
Они продаются либо в технических магазинах для автомобилей, либо в аптечных пунктах. Использовать можно как разбавленную кислотную массу, так и концентрированную
Со вторым вариантом настоятельно рекомендуется работать очень осторожно и соблюдать все техники и правила безопасности
Так как эта разновидность может моментально прожечь не только одежду, но и кожу. Выискивать требуемую плотность, можно при помощи инструкций, которые указаны на этикетке кислоты. Необходимо примерно разбавить нежное количество, а после этого при помощи ареометра, настроить точные параметры и свойства электролитической жидкости.
Разные аккумуляторные батареи требуют разное количество электролитического раствора. В среднестатистические аккумуляторы 50 — 75 Ампер-час, понадобится около 2,5 — 3,6 литров смеси. Различные ареометры.
Серная кислота в аккумуляторе
По сути то, что залито в аккумулятор — это разбавленная серная кислота. В основе работы любого свинцово-кислотного аккумулятора лежит химический процесс, высвобождающий электрический заряд. Молекулы серной кислоты расщепляют посредством электролитической диссоциации свинцовые электроды, создавая положительно и отрицательно заряженные ионы.
Собираясь на положительных и отрицательных электродах батареи, ионы создают на клеммах АКБ необходимый заряд. Со временем часть молекул связывается без возможности возобновить свою работу в банках, что снижает плотность электролита
Поэтому так важно следить за концентрацией аккумуляторной кислоты

Процесс носит название электролитической диссоциации. При нём ионы с положительным зарядом(катионы) — устремляются к плюсовому электроду. К отрицательному электроду направляются анионы — отрицательно заряженные ионы.
Окислителем выступает диоксид свинца, который в результате взаимодействия с молекулами кислоты восстанавливается, отдавая отрицательный заряд на электроды. Растворы серной кислоты слабо проводят электрический ток, однако хорошо справляется с ионным обменом.
При разрядке АКБ положительные ионы свинца устремляются через электролит с губчатого свинца – восстановителя. Здесь происходит превращение в двухвалентный свинец из четырехвалентного, таким образом, оставляя заряд 2 электронов с каждого иона.
На аноде — PbO2 + SO42− + 4H+ + 2e− -> PbSO4 + 2H2O — окисление свинца.
На катоде — Pb + SO42− − 2e− ->PbSO4
Во время зарядки идут обратные реакции — свинец движется в сторону пластин.

Оба электрода покрываются слоем сульфата, который образовывается из отрицательных кислотных остатков и положительных двухвалентных ионов свинца. Это называется сульфатацией, которая для пластин аккумулятора весьма опасна и грозит быстрым износом. Выделяемые газы в процессе восстановительно-окислительных реакций считаются побочным эффектом, однако они могут серьёзно повлиять на работоспособность всей батареи.
В процессе разрядки батареи к отрицательно заряженному электроду устремляются электроны, где они производят нейтрализацию ионов свинца. В зависимости от уровня заряда батареи плотность электролита может иметь разное значение.
Измерения делаются при комнатной температуре + 25 °С. Использование кислоты происходит в 1,6 раз больше положительными электродами. Поэтому рост объема электролита наблюдается при разрядке батареи и уменьшение – при зарядке.
Это интересно: Применение теплового насоса для отопления дома
Полная замена электролита в аккумуляторе
Электролит представляет смесь серной кислоты с водой в определенной пропорции. О концентрации раствора узнают по плотности, измеряемой ареометром. Показатель основной, даже сотые доли влияют на способность электролита работать на накопление энергии.

Признаки негодного электролита:
- Измерение плотности на заряженном аккумуляторе ареометром. Значение должно быть 1,25 -1,27 г/см3.
- Мутный электролит – свидетельство того что внутри идут паразитные процессы сульфатирования.
- Электролит перемерзал, но герметичность корпуса не нарушена.
- Раствор черный или темно-коричневый со взвесью угля и окалины.
Замена электролита в аккумуляторной батарее будет эффективна, когда полости банок обследованы, промыты, удален сульфатный осадок. Если разрушены пластины, осыпалось активное вещество – аккумулятор не ремонтопригоден.
В домашних условиях полная замена электролита в аккумуляторе автомобиля происходит в последовательности:
- Подготовить эмалированную или стеклянную посуду для слива электролита, средства личной защиты, место для работы, лучше, на открытом воздухе.
- Аккумулятор извлечь, из автомобиля, снять пробки или просверлить отверстия в необслуживаемом АКБ, слить жидкость в подготовленную тару, пользуясь грушей или шприцом.
- Аккумулятор промывается дистиллированной водой многократно, пока не удалится осадок. Возможно, придется удалять сульфат свинца, если есть осадок на пластинах. Нужно убедиться что активная замазка не осыпалась, угольная решетка цела.
- Медленно, с перерывами залить электролит нужной плотности в каждую банку выше пластин на 5-7 мм. Подождать 2-3 часа для выхода пузырьков, замерить плотность электролита, довести до нормы
- Зарядку аккумулятора после замены электролита вести малым током 0,1 А, не допуская закипания. После набора половины емкости, зарядка ведется циклично.
- Произвести герметизацию банок.

Сколько времени заряжать аккумулятор? Заряжать аккумулятор после замены электролита нужно бережно, как после глубокой разрядки. Операция замены электролита своими руками в автомобильном аккумуляторе считается законченной, если он полностью принимает ток длительное время
Зарядка ведется осторожно, кипение в банках недопустимо
Предлагаем посмотреть видео по правильной замене электролита в автомобильном аккумуляторе.
Процесс приготовления электролита

Электролит для АКБ можно, конечно, приобрести в специализированных магазинах, но можно сделать его самостоятельно и при этом научиться регулировать плотность.
Для приготовления электролита потребуются следующие компоненты:
- Вода дистиллированная.
- Серная кислота.
- Емкость из материала, устойчивого к воздействию концентрированного химического вещества: стекла, керамики, свинца.
- Эбонитовая палочка (для размешивания жидкости).
Для приготовления в специальную емкость заливается вода, после – серная кислота. Компоненты тщательно палочкой смешиваются. Процедуру проводят последовательно, поскольку при обратном варианте есть вероятность получить ожоги.
Полученное вещество плотно накрывается и оставляется минимум на сутки до выпадения осадка и остывания. Стоит знать, что при обратном проведении заливки (сначала серная кислота, потом – вода), возможна гидратации и образование в кислоте тепла. Соответственно, вода может закипеть и спровоцировать разбрызгивание.
Срок службы АКБ ограничен ее техническими характеристиками. Однако при неправильном его использовании и хранении этот показатель может существенно снизиться. Чтобы АКБ не изнашивалась слишком стремительно, специалисты рекомендуют следить за плотностью электролита и его уровнем.
Нейтрализация электролита
Если аккумулятор вышел полностью из строя, его требуется утилизировать грамотно. Но также в случае течи электролита из батареи необходимо узнать, чем нейтрализовать ее.
Бывают ситуации, когда при поломке аккумулятора может быть залита отдельная часть в месте его нахождения. Для этого необходимо вытащить батарею и провести очистку. Нейтрализация этого вещества из аккумулятора, как правило, проводится при помощи специального оборудования и применения технологий
Это важно с экономической и экологической точек зрения. Если проводить неорганизованную нейтрализацию, можно нанести значительный вред окружающей среде
В настоящее время имеются два варианта нейтрализующего вещества с кислотами промышленным способом. Первый предусматривает устранение фильтрующим методом сброса кислоты в стоки, с пропусканием через магнезит, известняк и другие материалы, а второй способ – регенерация кислоты специальной обработкой с последующим получением товарного продукта. Но на практике многие водители рекомендуют в случае пролива опасного вещества использовать щелочный раствор, который делается из пищевой соды и воды.
При регулярной проверке аккумулятора, в том числе контроле за плотностью и уровнем электролита, можно избежать многих проблем и продлить срок эксплуатации батареи, не допустить механических разрушений. Всегда требуется внимательно относиться к устройствам при эксплуатации, особенно в зимнее время, когда при низких температурах и сниженной плотности электролита может произойти его замерзание или разрушение пластин.
Как вам статья?
Мне нравитсяНе нравится
Какая кислота используется в автомобильных аккумуляторах
Большинство автомобилистов уверенно отвечают на этот вопрос, но есть и такие, которые с пеной у рта будут доказывать, что в батареях используется соляная кислота.
Строго говоря, актуальность этого вопроса практически нулевая: вам вряд ли придётся иметь дело с концентрированной кислотой. В магазинах и аптеках продаётся уже готовая жидкость, разбавленная в соотношении 65 частей воды на 35 частей кислоты.
Но это действительно серная кислота, не соляная. У химиков кислота, заливаемая в аккумулятор, называется специфически – триоксид серы или серный ангидрид, но мы будем придерживаться привычного нам термина.
Отметим, что хотя соляная кислота в качестве реагента в аккумуляторных батареях не используется, электролит бывает разным. Например, щелочным. Такие жидкости используются в никель-кидмиевых батареях. Более того, электролит бывает и не жидким, в виде пастообразного вещества с нулевой текучестью. Пример – гелевые АКБ, хотя это просто загущённый силиконовыми добавками обычный электролит.
Так что если вас спросят, какая кислота используется в аккумуляторе, серная или соляная, правильный ответ вы уже знаете.
Что касается соотношения между водой и кислотой, то пропорция 35:65 считается самой эффективной, но некоторые производители допускают применение ещё менее концентрированного раствора, в котором процентное содержание H2SO4 снижено до 30%.
Разумеется, знание того, какая кислота заливается в аккумулятор и каковы её пропорции – это хорошо, но для самостоятельного и правильного обслуживания кислотно-свинцовых аккумуляторов этого недостаточно.
Дело в том, что плотность электролита, которая напрямую зависит от соотношения компонентов, не является постоянной величиной. Мы уже рассказывали, что в процессе разряда кислоты становится меньше, при зарядке её количество восстанавливается.
Поэтому, когда говорят о плотности электролитической жидкости, подразумевают, что речь идёт о полностью заряженной АКБ. И если уровень жидкости оказался ниже требуемого, нужно сначала измерить плотность, чтобы знать, что доливать: воду или раствор кислоты.
Если плотность оказалась завышенной – в жидкость доливают дистиллированную воду, которая продаётся и в аптеках, и в автомагазинах (как и готовый электролит)
Процесс доливки описывать не имеет смысла, важно после этого зарядить батарею и снова измерить плотность раствора
Если мы выяснили, что в растворе мало кислоты, потребуется повысить её концентрацию, но делать это нужно, доливая готовый электролит. Добавлять в аккумулятор кислоту нельзя – это небезопасно и для вас, и для самого аккумулятора.
Впрочем, найти в продаже концентрированную кислоту не так просто, обычно она уже предлагается в виде растворов разной консистенции. Связано это с её высокой химической агрессивностью – при попадании на кожу сильнейшие ожоги неизбежны, опасен даже 35-процентный раствор.
Получают концентрированную серную кислоту поэтапно. Сначала готовят раствор с содержимым H2SO4 на уровне 60–70%, а затем доводят концентрацию до 98% – именно в таком виде она хранится дольше всего.
99-процентная серная кислота считается нестабильной, при длительном хранении она теряет часть сульфатного остатка, поэтому её концентрация всё равно падает до значений порядка 98.1–98.3%.

Кстати, существует около полутора десятков сортов серой кислоты. Приводим список наиболее распространённых:
- нитрозная, которую технари часто называют башенной. При концентрации 75% её плотность составляет 1.67 г/см3. Башенным сорт назвали из-за технологии изготовления с использованием футерованных башен, а нитрозным – из-за способа обработки посредством нитрозы с выходом серной кислоты и окисла азота;
- контактная, у которой плотность принимает значение 1.837 г/см3, а концентрация находится в пределах 92.4–98.0%. Этот вид также производят обжиговым способом, при котором газ, насыщенный двуокисью SO2, реагирует с катализатором на основе ванадия;
- аккумуляторная плотностью 1.835 г/см3, с содержимым серной кислоты 92–95%. Именно такая кислота обычно заливается в АКБ, будучи разбавленной до 35%;
- сорт олеум, или дымучая серная кислота – 100% H2SO4 с добавлением серного ангидрида – жидкость плотностью 1.897 г/см3;
- высокопроцентный олеум плотностью 2.002 г/см3, включающий до 65% свободного SO3.