Этиленгликоль опасность для человека
Содержание:
- К какому классу соединений относится этиленгликоль?
- Уникальные свойства этиленгликоля
- Использование этиленгликоля
- Кроме теплообменников, эта жидкость применяется в промышленности:
- Характеристика пропиленгликоля и глицерина
- Меры безопасности [ править | править код ]
- Первая помощь
- Применение
- Полезная информация
- Лечение отравления этиленгликолем
- История болезни
- Физические и теплофизическине свойства водных растворов глицерина
- Плотность водного раствора глицерина в зависимости от температуры и концентрации. Таблица.
- Концентрация глицерина по массе и по объёму в водном растворе
- Температура кипения смеси глицерина с водой (при нормальном атмосферном давлении)
- Температура замерзания смеси глицерина с водой (при нормальном атмосферном давлении)
- Производство
- Первая помощь и выведение вещества из организма
К какому классу соединений относится этиленгликоль?
16.12.2016 05:20
Использование этиленгликоля уверенно завоевывает огромную популярность в самых разных сферах промышленности. Это связано с легкостью его выработки и свойствами вещества. Что такое этиленгликоль и какой класс органических соединений? Бесцветная маслянистая жидкость не имеющая запаха сладковатая на вкус и относящаяся к классу многоатомных спиртов как раз и называется этиленгликолем. Она токсичная и отравление этим веществом может привести к летальному исходу. Однако спешим уверить, соблюдение правил безопасности при работе с продуктами на основе этиленгликоля исключает возможность угрозы, поэтому их нужно строго придерживаться.
Отравиться этиленгликолем можно и при употреблении внутрь, и при вдыхании паров. Первое делать ни в коем случае нельзя, от второго можно защититься специальными масками, которые рекомендуют надевать при тесном контакте с веществом.
Уникальные свойства этиленгликоля
-
Прекрасная растворимость в воде с абсолютно любой концентрацией (0%-100%).
-
Придание раствору особого качества: замерзание только при очень низких температурах (каких именно, напрямую зависит от концентрации вещества).
-
Гигроскопичность — прекрасно впитывает влагу и осушает поверхности.
-
Растворение в воде плохо или вообще нерастворимых веществ (гидрофобных и гидрофильных).
Использование этиленгликоля
-
Автомобильные антифризы.
-
Теплоноситель и хладоноситель (системы отопления, установки пищевой промышленности и так далее).
-
Производство разнообразных полимеров (полиуретан, целлофан и другие).
-
Растворитель красок.
-
В авиационном топливе.
-
Производство конденсаторов.
-
Криопротектор.
-
Для изготовления взрывчатого вещества нитрогликоля.
-
Системы чиллер-фанкойл (кондиционирование воздуха) — в качестве теплоносителя.
-
Крема для обуви (один из компонентов часто используемого товара).
-
Жидкость для мытья стекол (тоже один из компонентов).
Это еще не весь список продуктов, в состав которых входит этиленгликоль. Данное вещество применяется в лакокрасочной, косметической, металлургической, печатной и даже текстильной промышленности. Многие олифы, краски, эмали, смолы, защитные жидкости для кожи не обходятся без этиленгликоля. Эфиры этого вещества активно используют в создании косметических средств и парфюмерии.
Ценность этиленгликоля высока, поэтому сегодня его продают в чистом виде в большом количестве, благодаря чему активно развиваются разные сферы промышленности.
Кроме теплообменников, эта жидкость применяется в промышленности:
- химической,
- фармацевтической,
- текстильной,
- автомобильной,
- авиационной,
- электротехнической.
Полиуретаны, алкидные смолы и другая продукция содержит в своем составе раствор этиленгликоля. Как утверждает статистика, при этом доля антифризного направления составляет около 40%. И только производство синтетических полиэфирных волокон и пленок в мировом исчислении превышает этот показатель – 41-45%.
Несмотря на то, что впервые этот гликоль был получен еще в 1859 году, он сегодня с помощью улучшения состава считается одним из наиболее востребованных у потребителей незамерзающих веществ. Если гликоль купить для теплообменного оборудования, то это значительно сэкономит затраты в том числе и на обслуживание. Однако профилактика его должна проводиться во избежание ухудшения работы теплообменника. Необходимость замены гликоля возникает тогда, когда лабораторные анализы показывают снижение или полую утрату его эксплуатационных свойств.
Этиленгликоль вообще – это настолько благодатный материал, что разные отрасли промышленности нещадно пользуются любым его преимуществом. Например, такое качество, как гигроскопичность, не остается незамеченным и применяется для осушения газов, поглощения воды в трубном оборудовании для добычи газа в море. По сравнению с другими «конкурентами» этот теплоноситель имеет более структурированный диапазон применения.
Cодержание статьи: classList.toggle()»>развернуть
Этиленгликоль – одно из самых распространенных веществ, широко применяемых в быту и на производстве, относится к третьему классу опасности. Он входит в состав лаков и красок, средств бытовой химии, антифриза, пластмасс. Поэтому отравление этиленгликолем возникает довольно часто при нарушении правил его использования.
Этиленгликоль является токсичным веществом для организма, способным вызвать тяжелые отравления и даже смерть. По своей химической природе он относится к простым спиртам, без цвета и запаха, имеет легкую маслянистую консистенцию и сладковатый привкус. Это – еще один фактор, повышающий вероятность отравления
Поэтому очень важно предупредить интоксикацию и уметь правильно оказать первую помощь пострадавшему
Характеристика пропиленгликоля и глицерина
Пропиленгликоль (С3Н8О2) — это бесцветная жидкость. Его структурные характеристики таковы, что он является немного вязким, имеет слабый характерный запах и сладковатый вкус. Обладает гигроскопическими свойствами. В качестве добавки Е1520 пропиленгликоль разрешён в большинстве стран мира. Он считается нетоксичным веществом. При попадании на кожу или внутрь организма не вызывает раздражения и отравления. Удаляется при помощи воды.
У него можно выделить несколько основных физических свойств. К ним относятся:

- температура замерзания при -59;
- сохранение вкуса;
- удержание влаги;
- растворимость в воде;
- нетоксичность;
- антикоррозионность.
Способы получения
Основным способом получения пропиленгликоля или пропандиола является каталитическая гидратация окиси пропилена. Это осуществляется при температуре 150−220 градусов по Цельсию. У пропиленгликоля довольно широкий спектр применения, и его используют для производства следующих продуктов и веществ:

- антифризы;
- пищевые красители;
- крема и мази;
- пищевые ароматизаторы;
- жидкость для электронных сигарет.
Основными производителями в Европе являются компании Basf chemical и DWO Europe GMBH. Это вещество продаётся в основном под этими марками.
Свойства и использование глицерола
Глицерин — простейший представитель трёхатомных спиртов. Представляет собой вязкую бесцветную жидкость. Смешивается с водой в любых пропорциях. Если сравнить физические свойства основ, то даже без специальных исследований заметно, что этиленгликоль и пропиленгликоль во многом похожи, в отличие от глицерина. Последний даже при плюсовых температурах остаётся достаточно вязким.

Глицерин является довольно безвредным веществом. Он гигроскопичен, т. е. способен удерживать влагу, поглощая её, например, из воздуха. На этом свойстве основано его применение в косметической промышленности, где он используется для производства средств, увлажняющих кожу. Его также можно приобрести в аптеке, где он выпускается в качестве слабительных свечей или в жидком виде. Кроме того, глицерин используется в сельском хозяйстве для обработки семян и сеянцев деревьев. Это помогает прорастанию злаков и защищает кору деревьев от непогоды.
Меры безопасности [ править | править код ]
Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C. Температура самовоспламенения 380 °C. Температурные пределы воспламенения паров в воздухе, °С: нижний — 112, верхний — 124. Пределы воспламенения паров в воздухе от нижнего до верхнего, 3,8‒6,4% (по объему).
Этиленгликоль умеренно токсичен . По степени воздействия на организм относится к веществам 3-го класса опасности.
Летальная доза при однократном пероральном употреблении составляет 100‒300 мл этиленгликоля (1,5‒5 мл/кг массы тела) . Имеет относительно низкую летучесть при нормальной температуре, пары обладают не столь высокой токсичностью и представляют опасность лишь при хроническом вдыхании. Определённую опасность представляют туманы, однако при их вдыхании об опасности сигнализируют раздражение и кашель. Противоядием при отравлении этиленгликолем являются этанол и 4-метилпиразол .
В организме метаболизируется путём окисления до альдегида гликолевой кислоты и далее до гликолевой кислоты, которая затем распадается до муравьиной кислоты и диоксида углерода. Также он частично окисляется до щавелевой кислоты, которая вызывает повреждения почечной ткани. Этиленгликоль и его метаболиты выводятся из организма с мочой .
- Бесцветная, вязкая сиропообразная жидкость, сладкая на вкус. Не ядовит. Без запаха. Хорошо смешивается с водой.
- Распространён в живой природе. Играет важную роль в обменных процессах, так как входит в состав жиров (липидов) животных и растительных тканей.
В названиях многоатомных спиртов (полиолов) положение и число гидроксильных групп указывают соответствующими цифрами и суффиксами -диол (две ОН-группы), -триол (три ОН-группы) и т.д. Например:
Получение многоатомных спиртов
I . Получение двухатомных спиртов
1. Каталитическая гидратация оксида этилена (получение этиленгликоля):
2. Взаимодействие дигалогенпроизводных алканов с водными растворами щелочей:
II . Получение трёхатомных спиртов (глицерина)
Омыление жиров (триглицеридов):
Химические свойства многоатомных спиртов
1. С активными металлами:
2. С гидроксидом меди( II ) – качественная реакция!
1. С галогенводородными кислотами
Т ринитроглицерин — основа динамита
- Этиленгликольпроизводства лавсана, пластмасс, и для приготовления антифризов — водных растворов, замерзающих значительно ниже 0°С (использование их для охлаждения двигателей позволяет автомобилям работать в зимнее время); сырьё в органическом синтезе.
- Глицерин широко используется в кожевенной, текстильной промышленности при отделке кож и тканейи в других областях народного хозяйства. Сорбит(шестиатомный спирт) используется как заменитель сахара для больных диабетом. Глицерин находит широкое применение в косметике, пищевой промышленности, фармакологии, производстве взрывчатых веществ. Чистый нитроглицерин взрывается даже при слабом ударе; он служит сырьем для получения бездымных порохов и динамита― взрывчатого вещества, которое в отличие от нитроглицерина можно безопасно бросать. Динамит был изобретен Нобелем, который основал известную всему миру Нобелевскую премию за выдающиеся научные достижения в области физики, химии, медицины и экономики. Нитроглицерин токсичен, но в малых количествах служит лекарством, так как расширяет сердечные сосуды и тем самым улучшает кровоснабжение сердечной мышцы.
Первая помощь
При обнаружении пострадавшего с симптомами отравления этиленгликолем вызывайте бригаду скорой помощи. Времени на поход в поликлинику или вызов врача нет, нужна экстренная помощь, потому что интоксикация наступает моментально.
Доврачебная помощь:
- Обеспечьте больному свежий воздух, откройте окна или отведите на улицу.
- Давайте пить больше жидкости, чтобы увеличить диурез. Для питья подойдет теплый несладкий чай или обычная вода.
- Дайте сорбент (Полисорб, Активированный уголь), вызовите искусственную рвоту только если больной ведет себя адекватно и находится в сознании. Нарушается глотательный рефлекс, есть риск, что пострадавший захлебнется рвотными массами.
- Если пострадавший находится без сознания, освободите тело от сдавливающих элементов одежды (галстук) и положите больного на бок. При отсутствии сознания больше никаких реанимационных мероприятий до приезда скорой помощи не проводите.
- При попадании гликоля на слизистые оболочки (глаза) промойте пораженное место большим количеством воды.
До приезда бригады неотложной помощи постарайтесь выяснить у больного время приема токсической жидкости и объем принятого внутрь этиленгликоля. Сообщите врачам о наличии аллергии на медикаменты у пострадавшего.
Все остальные мероприятия делают медработники в условиях стационара.

Применение
Благодаря своей дешевизне этиленгликоль нашёл широкое применение в технике.
- Как компонент автомобильных антифризов и тормозных жидкостей, что составляет 60% его потребления. Смесь 60% этиленгликоля и 40% воды замерзает при −49 °С. Коррозионно активен, поэтому применяется с ингибиторами коррозии;
- Используется как теплоноситель с содержанием не более 50% в системах отопления (частные дома в основном)
- В качестве теплоносителя в виде раствора в автомобилях, в системах жидкостного охлаждения компьютеров;
- В производстве целлофана, полиуретанов и ряда других полимеров. Это второе основное применение;
- Как растворитель красящих веществ;
- В органическом синтезе:
- в качестве высокотемпературного растворителя.
- для защиты карбонильной группы путём получения 1,3-диоксолана. Обработкой вещества с карбонильной группой в бензоле или толуоле этиленгликолем в присутствии кислого катализатора (толуолсульфоновой кислоты, BF3•Et2O и др.) и азеотропной отгонкой на насадке Дина-Старка образующейся воды. Например, защита карбонильной группы изофорона

1,3-диоксоланы могут быть получены также при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана или комплекса диметилсульфат-ДМФА 1,3-диоксалана устойчивы к действию нуклеофилов и оснований. Легко регенерируют исходное карбонильное соединение в присутствии кислоты и воды.
- Как компонент противоводокристаллизационной жидкости «И».
- В качестве криопротектора.
- Для поглощения воды, для предотвращения образования гидрата метана (ингибитор гидратообразования), который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенерируют путём осушения и удаления солей.
- Этиленгликоль является исходным сырьём для производства взрывчатого веществанитрогликоля.
Этиленгликоль также применяется:
- при производстве конденсаторов
- при производстве 1,4-диоксана
- как теплоноситель в системах чиллер-фанкойл
- в качестве компонента крема для обуви (1‒2 %)
- в составе для мытья стёкол вместе с изопропиловым спиртом
- при криоконсервировании биологических объектов (в крионике) в качестве криопротектора.
- при производстве полиэтилентерефталата, пластика популярных ПЭТ-бутылок.
Полезная информация
Несмотря на то что этиленгликоль был получен ещё в 1859 году, он не сразу занял свою нишу в химии и промышленности. Изначально он использовался во времена Первой мировой войны, как замена глицерина, который широко применялся при производстве взрывчатых веществ.
Химическая формула данного простейшего многоатомного спирта – С2Н6О2 (иначе ее можно записать следующим образом – НО–СН2–СН2–ОН). Этиленгликоль имеет слегка сладковатый вкус, не имеет запаха, в очищенном состоянии выглядит, как немного маслянистая бесцветная прозрачная жидкость.
Основные химические и физические свойства 1,2-диоксиэтана:
- молярная масса – 62,068 г/моль;
- коэффициент оптического преломления – 1,4318;
- температура воспламенения – 124 градуса (верхний предел) и 112 градусов (нижний предел);
- температура самовоспламенения – 380 °С;
- температура замерзания (стопроцентный гликоль) – 22 °С;
- температура кипения – 197,3 °С;
- плотность – 11,113 г/кубический сантиметр.
Пары описываемого двухатомного спирта вспыхивают в тот момент, когда его температура достигает 120 градусов. Еще раз напомним, что 1,2-этандиол имеет 3-й класс опасности. А это означает, что его предельно допустимые концентрации в атмосфере могут быть не более 5 миллиграмм/кубический метр. Если же этиленгликоль попадает в организм человека, в нем могут развиться необратимые негативные явления, которые способны привести к смерти. При однократном употреблении вовнутрь 100 и более миллилитров гликоля наступает летальный исход.
Пары данного соединения менее токсичны. Так как этиленгликоль характеризуется сравнительно малым показателем летучести, реальная опасность для человека возникает тогда, когда он систематически вдыхает пары 1,2-этандиола. О том, что есть вероятность отравления парами (либо туманами) рассматриваемого соединения, сигнализирует кашель и раздражение слизистой оболочки. Если человек отравляется гликолем, ему следует принять препарат, содержащий 4-метилпиразол (мощный антидот, подавляющий фермент алкогольдегидрогеназы), или этанол (одноатомный этиловый спирт).
Этиленгликоль: что такое, применение, отравление — симптомы, первая помощь, лечение, профилактика
Что такое этиленгликоль — формула, получение, применение; влияние на организм человека, симптомы отравления, первая помощь, лечение, профилактика.

Отравление этиленгликолем
Отравление этиленгликолем. Симптомы, антидот. Прогноз и последствия для пациента.
Лечение отравления этиленгликолем
Первостепенные цели лечения
· Оказание первой помощи. Если с момента употребления вещества прошло не более 1 часа, необходимо вызвать рвоту чтобы очистить желудок и провести промывание большим количеством жидкости.
· Применить сорбенты для устранения токсинов из ЖКТ, например активированный уголь.
· Использовать слабительное. При этом обеспечить пациенту обильное питье, чтобы не допустить обезвоживание организма.
· Уменьшить ацидоз. Задержка деградации до токсичных метаболитов.
· При необходимости (наличию соответствующих симптомов) лечить гипокальциемию.
Первостепенно должны быть обеспечены жизненно важные функции пациента.
· Бикарбонат для уменьшения ацидоза.
· Применение этанола или другого антидота, чтобы задержать разложение этиленгликоля на токсичные метаболиты. Альтернативой является лечение антидотом фомепизолом.
· Гемодиализ удаляет этиленгликоль и гликолевую кислоту.
Схема лечения
· Гидрокарбонат натрия дозируется по кислотно-щелочному состоянию. Например, вне больницы. 250 ммоль (500 мл 4,2%) гидрокарбоната натрия вводят внутривенно при выраженной гипервентиляции.
· Кальций 9 мг / мл при симптоматической гипокальциемии 10 мл в / в более 2-3 мин.
· Диазепам (возможно, фенитоин) если судороги не отвечают на поставку кальция. Диазепам инъекция / клизма: 10-20 мг, при необходимости повторить.
· Этанол в качестве антидота вводят как перорально, так и в / в (та же доза), с целью терапевтической концентрации этанола ок. 1 ‰.
История болезни
Сбор анамнеза
У взрослых потребление обычно происходит в суицидальных целях или как альтернатива этанолу. Для составления истории болезни у пациента стоит уточнить наличие симптомов и следующую информацию:
- Количество и временной интервал проглатывания: когда и как долго пациент пил?
- Что употреблял вместе с этиленгликолем? Параллельный прием внутрь этанола снижает токсический эффект.
- Пациент также принимал таблетки или наркотики? Что и сколько?
- Могут ли окружающие люди также ошибочно выпить эту жидкость?
- Есть ли у человека хронические проблемы с алкоголем? Если да, то после лечения отравления ему стоит подобрать эффективный метод кодирования.
Физические и теплофизическине свойства водных растворов глицерина
Плотность водного раствора глицерина в зависимости от температуры и концентрации. Таблица.
Плотность смеси глицерина и воды приведена в таблице для концентрации глицерина от 10% до 70% по массе в диапазоне температур от нуля до ста градусов Цельсия.
| Температура, °C | Плотность водного раствора глицерина (содержание в процентах по массе) / ρ, г/см3 | ||||||
| 10% | 20% | 30% | 40% | 50% | 60% | 70% | |
| 1,025 | 1,052 | 1,079 | 1,107 | 1,135 | 1,163 | 1,192 | |
| 20 | 1,022 | 1,047 | 1,073 | 1,099 | 1,126 | 1,154 | 1,181 |
| 40 | 1,016 | 1,039 | 1,064 | 1,089 | 1,115 | 1,142 | 1,169 |
| 60 | 1,006 | 1,030 | 1,053 | 1,078 | 1,103 | 1,130 | 1,156 |
| 80 | 0,994 | 1,017 | 1,041 | 1,066 | 1.091 | 1,117 | 1.144 |
| 100 | 0,982 | 1,004 | 1,027 | 1,052 | 1,077 | 1,104 | 1,302 |
Вязкость водного раствора глицерина приводится в таблице в диапазоне температур смеси от нуля до ста градусов Цельсия и концентрации глицерина от 10% до 70%. Примечательно, что добавление всего лишь 10% (по массе) глицерина в воду позволяет повысить динамическую вязкость раствора на 30%.
| Температура, °C | Вязкость абсолютная (динамическая) водного раствора глицерина (содержание в процентах по массе) μ, Па*с | ||||||
| 10% | 20% | 30% | 40% | 50% | 60% | 70% | |
| 2,44*10-3 | 3,44*10-3 | 5,14*10-3 | 8,25*10-3 | 14,6*10-3 | 29,9*10-3 | 76,0*10-3 | |
| 20 | 1,31*10-3 | 1,76*10-3 | 2,5*10-3 | 3,72*10-3 | 6,0*10-3 | 10,8*10-3 | 22,5*10-3 |
| 40 | 0,826*10-3 | 1,07*10-3 | 1,46*10-3 | 2,07*10-3 | 3,10*10-3 | 5,08*10-3 | 9,4*10-3 |
| 60 | 0,575*10-3 | 0,731*10-3 | 0,956*10-3 | 1,30*10-3 | 1,86*10-3 | 2,85*10-3 | 4,86*10-3 |
| 80 | — | — | 0,69*10-3 | 0,918*10-3 | 1,25*10-3 | 1,84*10-3 | 2,9*10-3 |
| 100 | — | — | — | 0,668*10-3 | 0,91*10-3 | 1,28*10-3 | 1,93*10-3 |
Значения теплопроводности водного раствора глицерина показаны в таблице для диапазона температур от 20 до 80 градусов Цельсия и концентрации глицерина от 10% до 70%. С увеличением концентрации глицерина теплопроводность водного раствора снижается. При содержании 50% глицерина теплопроводность смеси примерно на 29% меньшей, чем у чистой воды.
| Температура | Теплопроводность смеси глицерина (содержание в процентах по массе) с водой Вт/(м*°C) | ||||||
| 10% | 20% | 30% | 40% | 50% | 60% | 70% | |
| 20 | 0,557 | 0,519 | 0,481 | 0,448 | 0,414 | 0,381 | 0,352 |
| 40 | 0,586 | 0,540 | 0,502 | 0,460 | 0,423 | 0,385 | 0,356 |
| 60 | 0,611 | 0,565 | 0,519 | 0,477 | 0,435 | 0,393 | 0,360 |
| 80 | 0,636 | 0,590 | 0,540 | 0,494 | 0,448 | 0,402 | 0,364 |
Оценочные значения теплоемкости водного раствора глицерина приводятся в таблице для температур от 20 до 80 градусов Цельсия и концентраций глицерина от 10 до 70%. С увеличением концентрации глицерина теплопроводность раствора снижается. При нормальных условиях и содержании 10% глицерина теплоемкость смеси примерно в 2 раза меньше теплоемкости чистой воды.
| Температура, °С | Теплоемкость смеси глицерина (содержание в процентах по массе) с водой кДж/(кг*°C) | ||||||
| 10% | 20% | 30% | 40% | 50% | 60% | 70% | |
| 20 | 1,998 | 1,907 | 1,816 | 1,725 | 1,634 | 1,542 | 1,452 |
| 40 | 2,002 | 1,916 | 1,830 | 1,744 | 1,659 | 1,573 | 1,487 |
| 60 | 2,010 | 1,929 | 1,848 | 1,767 | 1,687 | 1,606 | 1,525 |
| 80 | 2,024 | 1,948 | 1,871 | 1,795 | 1,718 | 1,642 | 1,608 |
Концентрация глицерина по массе и по объёму в водном растворе
В таблице ниже приведены соотношения концентрации глицерина в водном растворе по массе и по объёму.
| Концентрация глицерина в водном растворе по массе | 5% | 10% | 20% | 30% | 40% | 50% | 60% | 70% |
| Концентрация глицерина по объёму в водном растворе | 4,0% | 8,1% | 16,58% | 25,49% | 34,84% | 44,63% | 54,86% | 65,56% |
Температура кипения смеси глицерина с водой (при нормальном атмосферном давлении)
- Вода (без глицерина): 100°C
- Вода (90%) + Глицерин (10%): 100.7°C
- Вода (70%) + Глицерин (30%): 102,9°C
- Вода (50%) + Глицерин (50%): 106,7°C
- Глицерин (80%) + Вода (20%): 121,5°C
- Глицерин (90%) + Вода (10%): 139,8°C
- Глицерин (95%) + Вода (5%): 168 °C
Температура замерзания смеси глицерина с водой (при нормальном атмосферном давлении)
Источник, в основном: Богданов, Бурцев, Иванов, Куприянова «Холодильная Техника, Кондиционирование воздуха. Свойства веществ. » СПб. 1999
- Вода (90%) + Глицерин (10%): -2,2°C
- Вода (70%) + Глицерин (30%): -8,8°C
- Вода (50%) + Глицерин (50%): -21,4°C
- Глицерин (70%) + Вода (30%): -41,5°C
Производство
Промышленные маршруты
Этиленгликоль производят из этилена (этен), через промежуточное соединение этиленоксид. Оксид этилена реагирует с водой с образованием этиленгликоля в соответствии с химическим уравнением :
- C2H4O + H 2 O → HO-CH 2CH2-OH
Это реакция может катализироваться либо кислотами, либо основаниями, или может протекать при нейтральном pH при повышенных температурах. Наибольший выход этиленгликоля происходит при кислом или нейтральном pH с большим избытком воды. В этих условиях можно достичь выхода этиленгликоля 90%. Основными побочными продуктами являются олигомеры диэтиленгликоль, триэтиленгликоль и тетраэтиленгликоль. Разделение этих олигомеров и воды требует больших затрат энергии. Ежегодно производится около 6,7 миллионов тонн.
Более высокая селективность достигается за счет использования процесса OMEGA компании Shell. В процессе OMEGA оксид этилена сначала преобразуется с помощью диоксида углерода (CO. 2) в этиленкарбонат. Затем это кольцо гидролизуют основным катализатором на второй стадии с получением моноэтиленгликоля с селективностью 98%. На этом этапе снова выделяется диоксид углерода, который может быть снова подан в технологический контур. Углекислый газ частично поступает из производства окиси этилена, где часть этилена полностью окисляется.
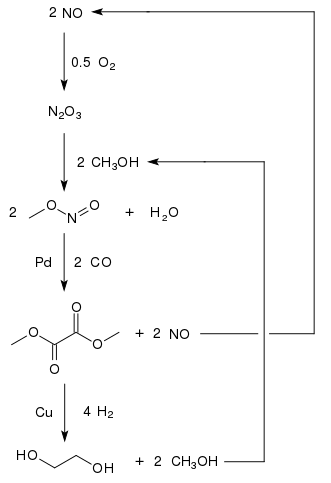
Этиленгликоль получают из окиси углерода в странах с большими запасами угля и менее строгими экологическими нормами. Окислительное карбонилирование метанола до диметилоксалата обеспечивает многообещающий подход к получению этиленгликоля на основе C 1. Диметилоксалат может быть преобразован в этиленгликоль с высокими выходами (94,7%) путем гидрирования с медным катализатором:
Поскольку метанол рециркулирует, потребляются только монооксид углерода, водород и кислород. Один завод с производственной мощностью 200 000 тонн этиленгликоля в год находится во Внутренней Монголии, а второй завод в китайской провинции Хэнань мощностью 250 000 тонн в год. год был намечен на 2012 год. По состоянию на 2015 год четыре завода в Китае мощностью 200 000 т / год каждый работали, и еще не менее 17 в будущем.
Биологические маршруты
55>гусеница большой восковой моли, Galleria mellonella, имеет кишечные бактерии, способные разлагать полиэтилен (PE) до этиленгликоля. 211>
Исторические маршруты
Согласно большинству источников, французский химик Шарль-Адольф Вюрц (1817–1884) впервые получил этиленгликоль в 1856 году. Он первым обработал «иодид этилена» ( C 2H4I2) ацетатом серебра и затем гидролизовали полученный «этилендиацетат» гидроксидом калия. Вюрц назвал свое новое соединение «гликоль», потому что он имеет общие свойства как с этиловым спиртом (с одной гидроксильной группой), так и с глицерином (с тремя гидроксильными группами). В 1859 году Вюрц получил этиленгликоль путем гидратации этиленоксида. По всей видимости, коммерческое производство или применение этиленгликоля не производилось до Первой мировой войны, когда он был синтезирован из этилендихлорида в Германии и использован в качестве заменителя глицерина. в индустрии взрывчатых веществ.
В Соединенных Штатах полукоммерческое производство этиленгликоля через этиленхлоргидрин началось в 1917 году. Первый крупномасштабный коммерческий завод по производству гликоля был построен в 1925 году в Южном Чарльстоне, Западная Вирджиния., компанией Carbide and Carbon Chemicals Co. (ныне Union Carbide Corp.). К 1929 году этиленгликоль использовался почти всеми производителями динамита. В 1937 году компания Carbide запустила первую установку, основанную на процессе Лефорта, для парофазного окисления этилена до окиси этилена. Carbide сохранял монополию на процесс прямого окисления до 1953 года, когда процесс научного проектирования был коммерциализирован и предложен для лицензирования.
Первая помощь и выведение вещества из организма
Алгоритм действий по оказанию помощи человеку, выпившему этиленгликоль или жидкость, его содержащую, таков:
- Вызвать бригаду скорой помощи;
- Промыть желудок содовым раствором (1 столовая ложка на 0,5 л воды);
- Давать обильное теплое питье: молоко, минеральная вода без газа;
- Дать выпить сорбент (активированный уголь, полисорб, энтеросгель);
- Дать слабительное, лучше всего подойдет магнезия.
Если пострадавший в сознании, и его состояние не тяжелое, хорошо дать выпить 100 мл водки или 50 мл медицинского спирта, разбавленного пополам с водой. Как это ни покажется странным, этиловый спирт является антидотом этого токсичного вещества, который можно применить в домашних условиях.
Если пострадавший без сознания, его нужно уложить на ровную поверхность, повернув голову набок во избежание асфиксии содержимым желудка в случае рвоты. Необходимо прощупать пульс и измерить давление. Пульс может быть нитевидным и даже не прощупываться на запястье, определять его нужно на сонных артериях – боковой поверхности шеи.
В случае остановки дыхания и отсутствия пульса нужно выполнить закрытый массаж сердца и принудительное искусственное дыхание.
В стационаре в качестве антидота при отравлении этиленгликолем вводится внутривенно стерильный щелочной раствор – бикарбонат натрия (сода), вводится глюконат кальция для восполнения его потери. Проводится восстановительная терапия, в зависимости от степени возникших нарушений. При тяжелом отравлении для очистки крови подключают аппарат гемосорбции (искусственная почка).