Этиленгликоль — строение, характеристика и классификация органического соединения
Содержание:
- Применение [ править | править код ]
- Применение
- Первое «знакомство» с этиленгликолем и глицерином: история получения
- Химические свойства одноатомных спиртов
- Что такое этиленгликоль
- Характеристика пропиленгликоля и глицерина
- Области применения и ценовая политика продукционного ряда
- Промышленное применение этиленгликоля
- Кроме теплообменников, эта жидкость применяется в промышленности:
- Характеристика пропиленгликоля и глицерина
- Особенности трёх спиртов
- Теплоносители в системах отопления
Применение [ править | править код ]
Благодаря своей дешевизне этиленгликоль нашёл широкое применение в технике.
- Как компонент автомобильных антифризов и тормозных жидкостей, что составляет 60% его потребления. Смесь 60% этиленгликоля и 40% воды замерзает при −49 °С. Коррозионно активен, поэтому применяется с ингибиторами коррозии;
- Используется как теплоноситель с содержанием не более 50% в системах отопления (частные дома в основном)
- В качестве теплоносителя в виде раствора в автомобилях, в системах жидкостного охлаждения компьютеров;
- В производстве целлофана, полиуретанов и ряда других полимеров. Это второе основное применение;
- Как растворитель красящих веществ;
- В органическом синтезе:
- в качестве высокотемпературного растворителя.
- для защиты карбонильной группы путём получения 1,3-диоксолана. Обработкой вещества с карбонильной группой в бензоле или толуоле этиленгликолем в присутствии кислого катализатора (толуолсульфоновой кислоты, BF3•Et2O и др.) и азеотропной отгонкой на насадке Дина-Старка образующейся воды. Например, защита карбонильной группы изофорона
1,3-диоксоланы могут быть получены также при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана или комплекса диметилсульфат-ДМФА 1,3-диоксалана устойчивы к действию нуклеофилов и оснований. Легко регенерируют исходное карбонильное соединение в присутствии кислоты и воды.
- Как компонент противоводокристаллизационной жидкости «И».
- В качестве криопротектора.
- Для поглощения воды, для предотвращения образования гидрата метана (ингибитор гидратообразования), который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенерируют путём осушения и удаления солей.
- Этиленгликоль является исходным сырьём для производства взрывчатого веществанитрогликоля.
Этиленгликоль также применяется:
- при производстве конденсаторов
- при производстве 1,4-диоксана
- как теплоноситель в системах чиллер-фанкойл
- в качестве компонента крема для обуви (1‒2 %)
- в составе для мытья стёкол вместе с изопропиловым спиртом
- при криоконсервировании биологических объектов (в крионике) в качестве криопротектора.
- при производстве полиэтилентерефталата, пластика популярных ПЭТ-бутылок.
Применение
Благодаря своей дешевизне этиленгликоль нашёл широкое применение в технике:
- Как компонент автомобильных антифризов и тормозных жидкостей, что составляет 60 % его потребления. Смесь 60 % этиленгликоля и 40 % воды замерзает при −45 °С. Коррозионно активен, поэтому применяется с ингибиторами коррозии;
- В качестве теплоносителя в виде раствора в автомобилях, в |системах жидкостного охлаждения компьютеров;
- В производстве целлофана, полиуретанов и ряда других полимеров. Это второе основное применение;
- Как растворитель красящих веществ;
- В органическом синтезе:
-
- в качестве высокотемпературного растворителя.
- для защиты карбонильной группы путём получения 1,3-диоксолана. Обработкой вещества с карбонильной группой в бензоле или толуоле этиленгликолем в присутствии кислого катализатора (толуолсульфоновой кислоты, BF3•Et2O и др.) и азеотропной отгонкой на насадке Дина-Старка образующейся воды. Например, защита карбонильной группы изофорона
1,3-диоксоланы могут быть получены также при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана или комплекса диметилсульфат-ДМФА
1,3-диоксалана устойчивы к действию нуклеофилов и оснований. Легко регенерируют исходное карбонильное соединение в присутствии кислоты и воды.
- Как компонент жидкости «И», используемой для предотвращения обводнения авиационных топлив.
- В качестве криопротектора
- Для поглощения воды, для предотвращения образования гидрата метана, который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенерируют путём осушения и удаления солей.
- Этиленгликоль является исходным сырьём для производства взрывчатого вещества нитрогликоля.
Этиленгликоль также применяется:
- при производстве конденсаторов
- при производстве 1,4-диоксана
- компонент в составе систем жидкостного охлаждения компьютеров
- как теплоноситель в системах чиллер-фанкойл
- в качестве компонента крема для обуви (1—2 %)
- в составе для мытья стёкол вместе с изопропиловым спиртом
Первое «знакомство» с этиленгликолем и глицерином: история получения
В 1859 году, посредством двухстадийного процесса взаимодействия дибромэтана с ацетатом серебра и последующей обработки едким кали полученного в первой реакции этиленгликольдиацетата, Шарль Вюрц впервые синтезировал этиленгликоль. Некоторое время спустя был разработан метод прямого гидролиза дибромэтана, но в промышленных масштабах в начале двадцатого века двухатомный спирт 1,2-диоксиэтан, он же – моноэтиленгликоль, или просто гликоль, в США получали посредством гидролиза этиленхлоргидрина.
На сегодняшний день и в промышленности, и в лаборатории применяют ряд других методов, новых, более экономичных с сырьевой и энергетической точек зрения, и экологичных, так как применение реагентов, содержащих или выделяющих хлор, токсины, канцерогены и другие опасные для окружающей среды и человека вещества, сокращается по мере развития «зелёной» химии.

Аптекарем Карлом Вильгельмом Шееле в 1779 году был открыт глицерин, а особенности состава соединения изучил в 1836 году Теофиль Жуль Пелуз. Двумя десятилетиями позже было установлено и обосновано строение молекулы данного трёхатомного спирта в трудах Пьера Эжена Марселея Вертело и Шарля Вюрца. Наконец, ещё двадцать лет спустя Шарль Фридель провёл полный синтез глицерина. В настоящее время промышленность использует два метода его получения: через хлористый аллил из пропилена, а также через акролеин. Химические свойства этиленгиликоля, как и глицерина, широко используют в различных сферах химического производства.
Химические свойства одноатомных спиртов
Общая формула одноатомных предельных спиртов: CnH2n+1OH. В спиртах, одноатомных и многоатомных, помимо связи между углеродом и водородом (С—ОН), есть еще одна связь между кислородом и водородом (О—Н). Поэтому химические реакции проходят с разрывом одной из цепей:
-
реакции восстановления проходят с отщеплением гидроксильной группы от молекулы спирта;
-
реакции окисления — с отщеплением водорода.
Низшие спирты (метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин) смешиваются с водой в любых соотношениях.
Кислотно-основные свойства
Согласно теории Бренстеда-Лоури спирты — достаточно слабые кислоты. Кислотность спиртов уменьшается по мере усложнения углеродного скелета.
-
Взаимодействие со щелочными металлами:
2С2Н5ОН + 2Na → 2C2H5ONa + H2. -
Взаимодействие со щелочами:
С2H5OH + NaOH ⇄ C2H5ONa + H2O.
Спирты — более слабые кислоты, чем вода, поэтому невозможна реакция с водными растворами щелочей. Взаимодействие с твердыми щелочами возможно, реакция обратима. Равновесие сильно смещено влево.
Основность кислот увеличивается по мере увеличения углеродного скелета.
Замещение гидроксогруппы
Гидроксогруппа является плохо уходящей. Энергия разрыва связи С—О довольно высока, поэтому непосредственное замещение группы ОН на другую группу невозможно.
Для того, чтобы замещение было возможно, группу ОН превращают в хорошо уходящую, т. е. понижают энергию разрыва связи. Для этого:
-
проводят реакцию в кислой среде;
-
переводят гидроксигруппу в сульфогруппу применяя H2SO4;
-
применяют кислоты Льюиса.
R—OH + PCl5 → R—Cl + POCl3 + HCl
R—OH + SOCl2 → R—Cl + SO2 + HCl
R—OH + HCl → R—Cl + H2O
R—OH + PBr → R—Br + H3PO3
R—OH + KBr + H2SO4 → R—Br + KHSO4 + H2O
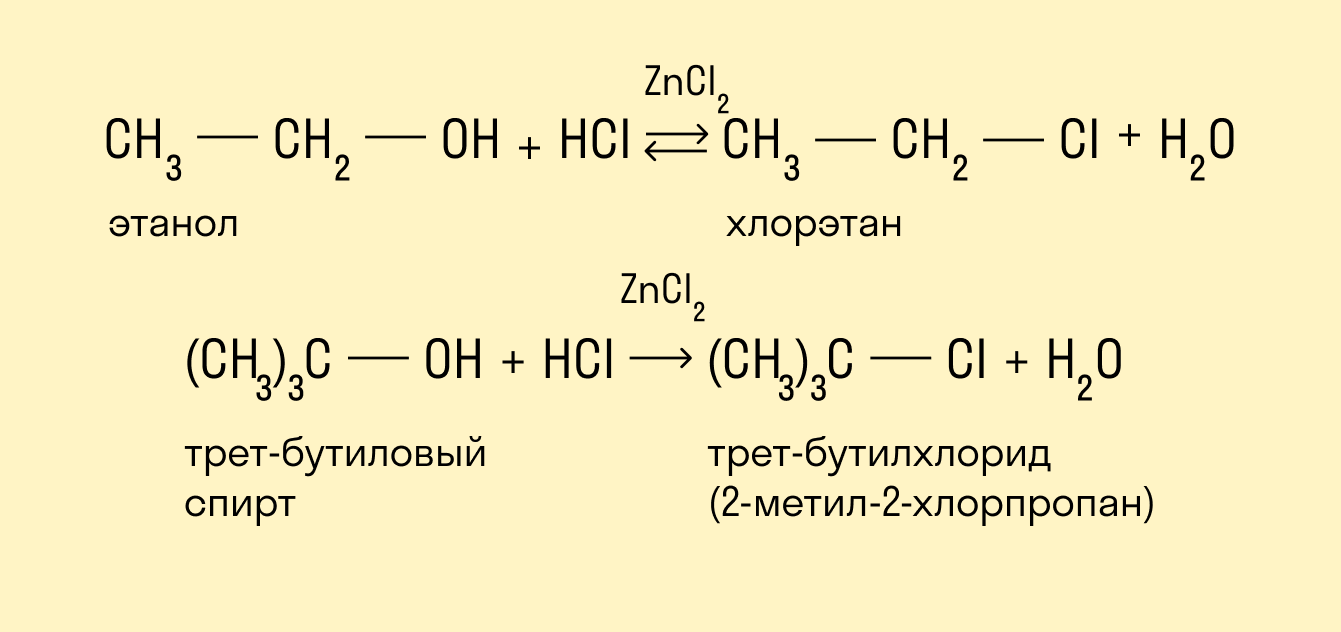
Реакция с использованием реактива Лукаса
Реактив Лукаса — это смесь ZnCl2 и HCl. Скорость реакции убывает при упрощении углеродного скелета. Внешним признаком реакции служит расслоение реакционной смеси в случае образования хлоруглеводорода R—Cl, представляющего собой маслообразное нерастворимое вещество.
Быстрее всего реагируют третичные спирты, слой нерастворимого алкилгалогенида появляется фактически сразу же после смешения реагентов — меньше чем за минуту.
Вторичные спирты вначале растворяются в реактиве, но затем раствор мутнеет, в течение 5 минут появляются капли алкилгалогенида.
Растворы первичных спиртов остаются прозрачными, они образуют хлориды только при нагревании.
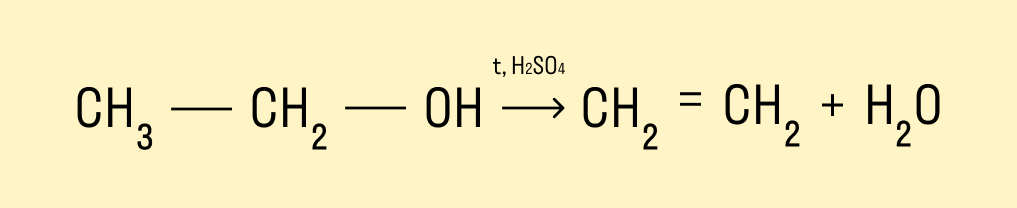
Дегидратация спиртов
При температуре &rt; 140°C и в присутствии серной кислоты происходит внутримолекулярная дегидратация. В результате реакции получается алкен.
При температуре < 140°C и в присутствии серной кислоты происходит межмолекулярная дегидратация. В результате образуется простой эфир.
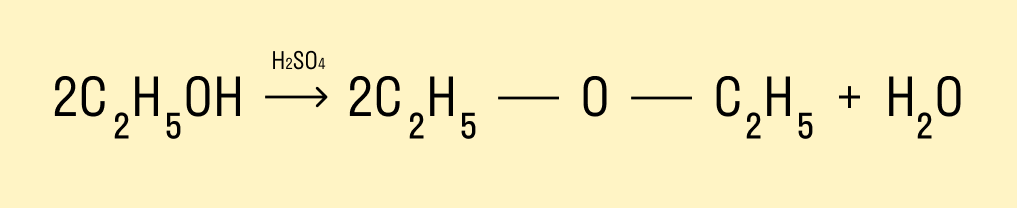
Реакция этерификации — получение сложных эфиров
Предельные одноатомные спирты вступают в химические реакции с карбоновыми кислотами, продукты таких реакций — сложные эфиры.
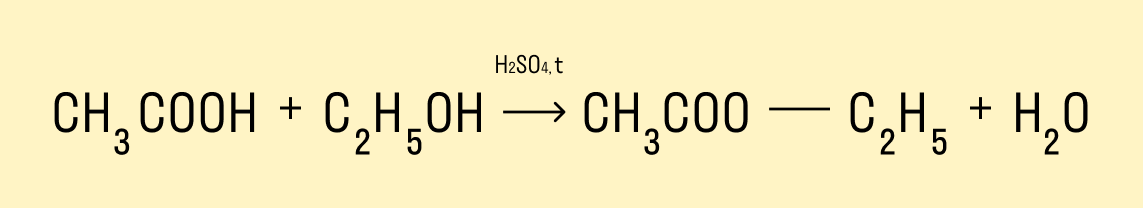
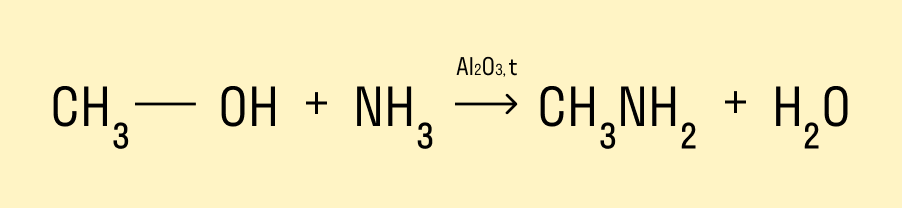
Взаимодействие с аммиаком
Эта реакция происходит при нагревании и в присутствии катализатора. Гидроксогруппа замещается на аминогруппу. Продукт реакции — амин.
Окисление
-
Горение спиртов:
C2H5OH + 3O2 → 2CO2 + 3H2O. -
Жидкофазное окисление с применением хромовой смеси K2Cr2O7 + H2SO4:
3C2H5OH + K2Cr2O7 + 4H2SO4 → 3CH3COOH + K2SO4 + Cr2(SO4)3 + H2O. -
Окисление оксидом меди (II) при нагревании:
CH3—CH2—OH + CuO → CH3—CHO + Cu + H2O.
Первичные спирты при окислении образуют альдегиды, вторичные переходят в кетоны, третичные окисляются с разрушением углеродного скелета.
Что такое этиленгликоль
Этиленгликоль — это представитель спиртов с двумя метильными группами в своём составе. Но в отличие от других он имеет немного маслянистую консистенцию.
Несмотря на то что этиленгликоль был получен ещё в 1859 году, он не сразу занял свою нишу в химии и промышленности. Изначально он использовался во времена Первой мировой войны, как замена глицерина, который широко применялся при производстве взрывчатых веществ.
Химическая формула этиленгликоля — C2H6O2, рациональная — С2Н4(ОН)2. По своим физическим свойствам — это жидкость без запаха, но со сладким вкусом. Он легко соединяется с водой в любой консистенции, что успешно применяется в промышленности, ведь температура замерзания таких жидкостей очень низкая — это улучшает свойства «незамерзаек».
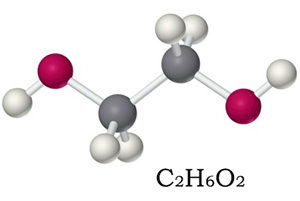 У этиленгликоля есть несколько названий, которые нередко можно встретить в составе продуктов химического производства:
У этиленгликоля есть несколько названий, которые нередко можно встретить в составе продуктов химического производства:
- гликоль;
- этандиол-1,2;
- 1,2-диоксиэтан.
Чаще других употребляется основное название.
К какому классу опасности относится этиленгликоль? — к умеренно токсичное легковоспламеняющееся вещество.
Способы получения
Производством этиленгликоля в промышленных масштабах занялись ещё в тридцатые годы прошлого века. Одним из способов его получения тогда было окисление этилена до его оксида. Около 20 лет такой метод оставался единственным.
Немного позже этиленгликоль стали получать с помощью насыщения оксида этилена водой, в присутствии серной и ортофосфорной кислот. Этот способ оказался выгодней предыдущего, так как на выходе производили более 90% этиленгликоля с минимальным количеством примесей.
Где применяется
В основном этиленгликоль используют в промышленности для обработки техники, что обусловлено его стоимостью — это недорогой и всем доступный продукт.
 Он выпускается в химической промышленности для ухода за автомобилями:
Он выпускается в химической промышленности для ухода за автомобилями:
- более 50% вещества идёт на создание тормозных жидкостей и антифризов, так как смесь гликоля и воды способна сохранять жидкую консистенцию даже при 40º C ниже нуля;
- этиленгликоль входит в состав охлаждающей жидкости — тосола;
- он может устранять коррозию, поэтому гликоль добавляют в антикоррозийные химические соединения.
Где ещё используется этиленгликоль?
- Его можно обнаружить в составе антистатиков.
- Используют для производства средств защиты против обледенения.
- Служит смазкой в холодильных установках.
- Находит применение этиленгликоль как наполнитель в гидравлических системах.
- Гликоль нередко используют для дезинфекции больших помещений.
- Одно из ключевых применений вещества — это производство бытовых химических продуктов, к числу которых относится целлофан, полиуретан.
- Он используется не только при охлаждении автомобилей, но и компьютеров.
- Этиленгликоль или химические соединения в составе с ним применяется, как средство для чистки автомобильных стёкол и зеркал.
- В небольшом количестве присутствует в креме для обработки обуви.
- Применяется этиленгликоль и в медицине, как составная часть криопротекторов для тканей и органов. То есть веществ, которые используют для заморозки.
- Это один из компонентов конденсаторов.
- Ключевым свойством этиленгликоля является поглощение воды, что успешно используется, чтобы предотвратить обледенение топлива в авиации и синтеза гидрата метана в трубопроводах, которые проходят в море.
- В органической химии его применяют как высокотемпературный растворитель.
- Без него не проходит синтез химических соединений.
- Где ещё используется этиленгликоль? — даже в наше время с его участием создают взрывчатые вещества.
За прошедшие десятилетия для этого двухатомного спирта нашлось множество применений, что, конечно же, обусловлено его свойствами. Но в медицине он известен не только как полезный и нужный продукт в быту, но и как средство, после контакта с которым человек может умереть.
Так что это такое этиленгликоль? — полезное химическое вещество, без которого не обходится производство большинства органических соединений или сильнодействующий яд с мощным отравляющим эффектом? Давайте узнаем, как может повлиять этиленгликоль на человека.
Характеристика пропиленгликоля и глицерина
Пропиленгликоль (С3Н8О2) — это бесцветная жидкость. Его структурные характеристики таковы, что он является немного вязким, имеет слабый характерный запах и сладковатый вкус. Обладает гигроскопическими свойствами. В качестве добавки Е1520 пропиленгликоль разрешён в большинстве стран мира. Он считается нетоксичным веществом. При попадании на кожу или внутрь организма не вызывает раздражения и отравления. Удаляется при помощи воды.
У него можно выделить несколько основных физических свойств. К ним относятся:

- температура замерзания при -59;
- сохранение вкуса;
- удержание влаги;
- растворимость в воде;
- нетоксичность;
- антикоррозионность.
Способы получения
Основным способом получения пропиленгликоля или пропандиола является каталитическая гидратация окиси пропилена. Это осуществляется при температуре 150−220 градусов по Цельсию. У пропиленгликоля довольно широкий спектр применения, и его используют для производства следующих продуктов и веществ:

- антифризы;
- пищевые красители;
- крема и мази;
- пищевые ароматизаторы;
- жидкость для электронных сигарет.
Основными производителями в Европе являются компании Basf chemical и DWO Europe GMBH. Это вещество продаётся в основном под этими марками.
Свойства и использование глицерола
Глицерин — простейший представитель трёхатомных спиртов. Представляет собой вязкую бесцветную жидкость. Смешивается с водой в любых пропорциях. Если сравнить физические свойства основ, то даже без специальных исследований заметно, что этиленгликоль и пропиленгликоль во многом похожи, в отличие от глицерина. Последний даже при плюсовых температурах остаётся достаточно вязким.

Глицерин является довольно безвредным веществом. Он гигроскопичен, т. е. способен удерживать влагу, поглощая её, например, из воздуха. На этом свойстве основано его применение в косметической промышленности, где он используется для производства средств, увлажняющих кожу. Его также можно приобрести в аптеке, где он выпускается в качестве слабительных свечей или в жидком виде. Кроме того, глицерин используется в сельском хозяйстве для обработки семян и сеянцев деревьев. Это помогает прорастанию злаков и защищает кору деревьев от непогоды.
Области применения и ценовая политика продукционного ряда
Стоимость на заводах и предприятиях, занимающихся производством и продажей подобных реактивов, колеблется в среднем около 100 рублей за килограмм такого химического соединения, как этиленгликоль. Цена зависит от чистоты вещества и максимального процентного содержания целевого продукта.

Применение этиленгликоля не ограничивается какой-то одной областью. Так, в качестве сырья его используют в производстве органических растворителей, искусственных смол и волокон, жидкостей, замерзающих при отрицательных температурах. Он задействован во многих промышленных отраслях, таких как автомобильная, авиационная, фармацевтическая, электротехническая, кожевенная, табачная. Неоспоримо весомо его значение для органического синтеза.
Важно помнить, что гликоль – это токсичное соединение, которое может нанести непоправимый вред здоровью человека. Поэтому его хранят в герметичных сосудах из алюминия или стали с обязательным внутренним слоем, защищающим ёмкость от коррозии, только в вертикальных положениях и помещениях, не снабженных отопительными системами, но с хорошей вентиляцией
Срок – не более пяти лет.
Промышленное применение этиленгликоля
Этандиол используется для производства различных материалов и веществ. К ним относятся:

- охлаждающие жидкости и антифризы на основе этиленгликоля;
- целлофаны;
- полиуретаны;
- конденсаторы;
- тормозные жидкости;
- теплоносители.
В частности, он активно применяется для создания антифризов. Продукт на основе этого спирта не замерзает, даже если его охлаждать до -40. Вещество становится только более вязким, сохраняя при этом свою текучесть. Для того чтобы полностью кристаллизоваться, температура нужна ещё ниже, потому что процесс кристаллизации у него довольно длительный.
Кроме теплообменников, эта жидкость применяется в промышленности:
- химической,
- фармацевтической,
- текстильной,
- автомобильной,
- авиационной,
- электротехнической.
Полиуретаны, алкидные смолы и другая продукция содержит в своем составе раствор этиленгликоля. Как утверждает статистика, при этом доля антифризного направления составляет около 40%. И только производство синтетических полиэфирных волокон и пленок в мировом исчислении превышает этот показатель – 41-45%.
Несмотря на то, что впервые этот гликоль был получен еще в 1859 году, он сегодня с помощью улучшения состава считается одним из наиболее востребованных у потребителей незамерзающих веществ. Если гликоль купить для теплообменного оборудования, то это значительно сэкономит затраты в том числе и на обслуживание. Однако профилактика его должна проводиться во избежание ухудшения работы теплообменника. Необходимость замены гликоля возникает тогда, когда лабораторные анализы показывают снижение или полую утрату его эксплуатационных свойств.
Этиленгликоль вообще – это настолько благодатный материал, что разные отрасли промышленности нещадно пользуются любым его преимуществом. Например, такое качество, как гигроскопичность, не остается незамеченным и применяется для осушения газов, поглощения воды в трубном оборудовании для добычи газа в море. По сравнению с другими «конкурентами» этот теплоноситель имеет более структурированный диапазон применения.
Cодержание статьи: classList.toggle()»>развернуть
Этиленгликоль – одно из самых распространенных веществ, широко применяемых в быту и на производстве, относится к третьему классу опасности. Он входит в состав лаков и красок, средств бытовой химии, антифриза, пластмасс. Поэтому отравление этиленгликолем возникает довольно часто при нарушении правил его использования.
Этиленгликоль является токсичным веществом для организма, способным вызвать тяжелые отравления и даже смерть. По своей химической природе он относится к простым спиртам, без цвета и запаха, имеет легкую маслянистую консистенцию и сладковатый привкус. Это – еще один фактор, повышающий вероятность отравления
Поэтому очень важно предупредить интоксикацию и уметь правильно оказать первую помощь пострадавшему
Характеристика пропиленгликоля и глицерина
Пропиленгликоль (С3Н8О2) — это бесцветная жидкость. Его структурные характеристики таковы, что он является немного вязким, имеет слабый характерный запах и сладковатый вкус. Обладает гигроскопическими свойствами. В качестве добавки Е1520 пропиленгликоль разрешён в большинстве стран мира. Он считается нетоксичным веществом. При попадании на кожу или внутрь организма не вызывает раздражения и отравления. Удаляется при помощи воды.
У него можно выделить несколько основных физических свойств. К ним относятся:

- температура замерзания при -59;
- сохранение вкуса;
- удержание влаги;
- растворимость в воде;
- нетоксичность;
- антикоррозионность.
Способы получения
Основным способом получения пропиленгликоля или пропандиола является каталитическая гидратация окиси пропилена. Это осуществляется при температуре 150−220 градусов по Цельсию. У пропиленгликоля довольно широкий спектр применения, и его используют для производства следующих продуктов и веществ:

- антифризы;
- пищевые красители;
- крема и мази;
- пищевые ароматизаторы;
- жидкость для электронных сигарет.
Основными производителями в Европе являются компании Basf chemical и DWO Europe GMBH. Это вещество продаётся в основном под этими марками.
Свойства и использование глицерола
Глицерин — простейший представитель трёхатомных спиртов. Представляет собой вязкую бесцветную жидкость. Смешивается с водой в любых пропорциях. Если сравнить физические свойства основ, то даже без специальных исследований заметно, что этиленгликоль и пропиленгликоль во многом похожи, в отличие от глицерина. Последний даже при плюсовых температурах остаётся достаточно вязким.

Глицерин является довольно безвредным веществом. Он гигроскопичен, т. е. способен удерживать влагу, поглощая её, например, из воздуха. На этом свойстве основано его применение в косметической промышленности, где он используется для производства средств, увлажняющих кожу. Его также можно приобрести в аптеке, где он выпускается в качестве слабительных свечей или в жидком виде. Кроме того, глицерин используется в сельском хозяйстве для обработки семян и сеянцев деревьев. Это помогает прорастанию злаков и защищает кору деревьев от непогоды.
Особенности трёх спиртов
Спирты — это функциональные производные углеводородов, имеющие в своём составе гидроксильную группу. Если она одна, то это одноатомные спирты, если гидроксигрупп несколько, то это многоатомные спирты. Например, в молекуле этандиола-1,2 две гидроксильные группы:
НО — СН2 — СН2 — ОН
В молекуле пропантриола-1,2,3 три гидроксильные группы. Соответственно, он является трёхатомным спиртом:
НО — СН2 — ОН — СН — СН2 — ОН
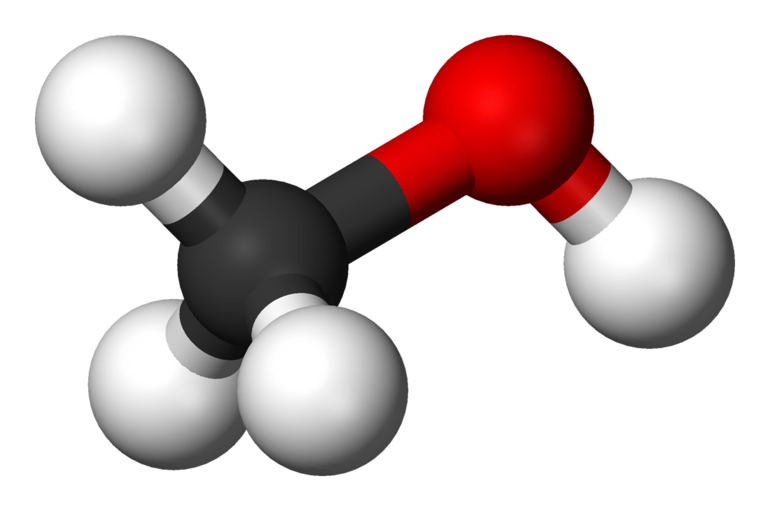
Вещества, содержащие несколько ОН-групп одного атома углерода, не относятся к классу спиртов и в большинстве случаев очень неустойчивы. В результате отщепления воды они превращаются в карбонильные соединения: СН3 — ОН — СН — ОН (гидрат ацетальдегида) = С2Н4О (ацетальдегид или этаналь) + Н2О (вода).
Из спиртов выделяются два представителя: этандиол-1,2 (c2h6o2) и пропантриол-1,2,3 (С3Н8О3). Название многоатомных спиртов строится так же, как и одноатомных. Сначала идёт название соответствующего алкана, на конце «ол», а перед ним располагается суффикс, обозначающий количество гидроксигрупп (ди, три, тетра). Например, диэтиленгликоль, триэтандиол, триэтиленгликоль и др.
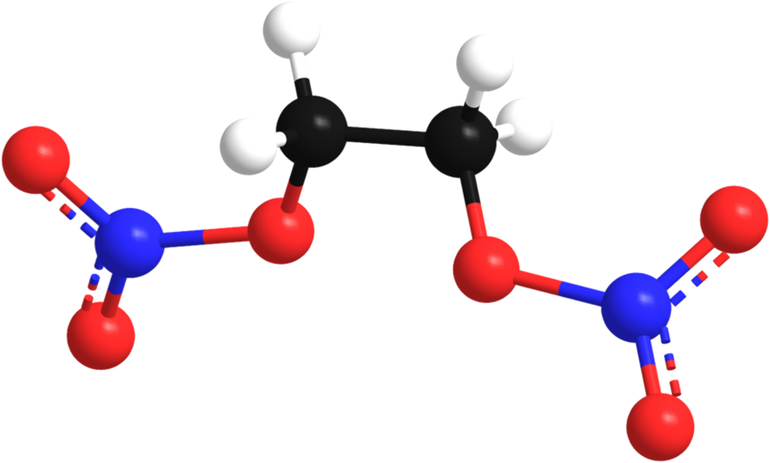
Этандиол имеет ещё одно название — этиленгликоль, а пропантриол — это тот же глицерин или глицерол. В целом двухатомные спирты часто называют гликолями. Этиленгликолевый раствор (смешанный с водой) замерзает при температурах ниже 40 градусов, поэтому он используется в системе охлаждения двигателей у автомобилей в зимний период.
Этиленгликоль, формула которого С2Н6О2, является простейшим видом спиртов. В очищенном виде он представляет собой прозрачную бесцветную жидкость, слегка маслянистой консистенции. Он не имеет запаха и обладает сладковатым вкусом; токсичен. Попадание этиленгликоля или его растворов в организм человека может вызвать необратимые изменения и привести к смерти.
Теплоносители в системах отопления
Состав любого теплоносителя условно можно разделить на четыре составляющие. К ним относятся:

- основа (одна из разновидностей гликолей и полигликолей);
- красители;
- пакет присадок;
- специально подготовленная деминерализованная (дистиллированная) вода.
В состав основы может входить один из трёх спиртов: глицерин, пропиленгликоль, этиленгликоль. Разумеется, если просто перемешать все эти компоненты в домашних условиях, то вместо теплоносителя можно получить бесполезную цветную жидкость с нерастворённой взвесью. Производство теплоносителя — это сложный процесс, осуществляемый в промышленных условиях с соблюдением ГОСТа, многочисленных рецептур и технических требований под контролем высококвалифицированных специалистов.
Основные плюсы этандиола
Отличительной характеристикой теплоносителя на основе этиленгликоля является то, что он устойчив к низким температурам и замерзает при -65 градусах (в зависимости от концентрации). Входящие в их состав присадки предотвращают образование накипи и коррозии в трубах. В отличие от других теплоносителей, например, воды, водногликолевые растворы при замерзании расширяются всего на 1,5−2%, что не оказывает негативного влияния на работу тепловых систем.
Обычно чистый концентрат никогда не заливают и смешивают его с дистиллированной водой в пропорции 60 на 40 или 50/50.
Между моноэтиленгликолем и этиленгликолем разницы практически нет — это прозрачная вязкая жидкость, относящаяся к спиртам. К минусам такого теплоносителя относят его токсичность. Попадание 0,1 литра этой жидкости внутрь организма может привести к летальному исходу. Однако при соблюдении эксплуатационных требований и герметичности контура его утечек можно избежать. Всё же по некоторым предписаниям он не применяется в системах отопления детского сада и в некоторых других муниципальных и технических объектах, т. к. в случае утечки это может привести к отравлению людей.
Альтернативная жидкость
Как следствие, позже был изобретён теплоноситель на основе пропиленгликоля. Отличить его можно по специальной маркировке, на которой указана температура замерзания (до минус 30). Пропиленгликоль используется для производства массы продуктов не только в химической, но и в пищевой промышленности. Из него производят добавку Е1520, а также при смешивании с глицерином 50/50 добавляют в электронные сигареты. Иными словами, он совершенно безвреден.

Единственным его минусом является цена, т. к. у такого экологического теплоносителя она будет в два раза больше. Фактически 10 кг этиленгликоля и пропиленгликоля стоят одинаково, однако первый можно разводить с водой почти в два раза, что является намного выгоднее.
У теплоносителя как на основе этиленгликоля, так и на основе пропиленгликоля теплоёмкость гораздо ниже. Соответственно, при проектировании системы отопления следует закладывать большее количество секций радиаторов для создания большей теплоотдачи. Вязкость и плотность у этих теплоносителей также в два-три раза выше, чем у воды, поэтому циркуляционные насосы также следует закладывать больше и мощнее.
Это не касается домов большой площади, т. к. там уже рассчитаны насосы с больши́м запасом.
У пропиленгликоля довольно большое объёмное расширение, и расширительный бак для него необходим большего размера. Кроме того, эти спирты запрещают использовать в качестве теплоносителей большинство производителей газовых и электрических котлов, т. к. их кислотность не всегда совместима с прокладками и теплообменниками. Они также не очень хорошо «дружат» с алюминиевыми радиаторами и межсекционными прокладками, опять же из-за высокой кислотности. Во время эксплуатации их будет разъедать. Отсюда лучше использовать либо литые, либо стальные панельные радиаторы.

Так как этиленгликоль является ядовитым веществом, то утилизировать теплоноситель на его основе (после окончания срока службы) необходимо специальным способом. Существуют определённые компании, которые занимаются его утилизацией. Попросту сливать этиленгликоль в почву крайне не рекомендуется.
Конечно, для хорошей циркуляции по узким каналам отопительного оборудования необходим теплоноситель с самой лучшей текучестью и минимальной вязкостью